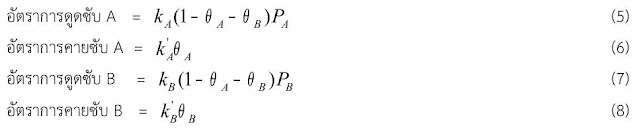ไอโซเทอมการดูดซับของ
Langmuir
(Langmuir isotherm) ถูกนำเสนอโดย
Irving
Langmuir ในปีค.ศ.
๑๙๑๖
แบบจำลองนี้เป็นแบบจำลองที่ง่ายที่สุดและเป็นแบบจำลองแบบแรกที่ได้รับการเสนอขึ้นมาโดยอาศัยพื้นฐานทางทฤษฎี
จากการที่กแบบจำลองนี้มีความเรียบง่ายจึงมักถูกใช้เป็นสมการเริ่มต้นในการสร้างแบบจำลองการเกิดปฏิกิริยาต่าง
ๆ
ไอโซเทอมการดูดซับของ
Langmuir
มีข้อสมมุติดังนี้
1.
สารที่ถูกดูดซับ
(adsorbed
species)
จะถูกยึดไว้ที่ตำแหน่งใดตำแหน่งหนึ่งบนพื้นผิวเท่านั้น
(หมายความว่าการดูดซับสามารถเกิดได้มากที่สุด
และมีความหนาเพียงชั้นเดียว)
แต่ละตำแหน่งจะสามารถจับสารที่ถูกดูดซับได้เพียงตัวเดียวเท่านั้น
2.
ความแตกต่างระหว่างพลังงานของการดูดซับจะไม่ขึ้นกับปริมาณของสารที่ถูกดูดซับลงไปบนพื้นผิวก่อนหน้า
ข้อสมมุติข้อนี้หมายความว่าพื้นผิวดูดซับมีลักษณะที่เหมือนกันหมด
ไม่มีแรงกระทำระหว่างโมเลกุลที่ลงไปเกาะก่อนกับโมเลกุลที่กำลังจะลงไปเกาะ
ตัวอย่างรูปแบบของสมการคณิตศาสตร์การดูดซับตามแบบจำลองของ
Langmuir
(ก)
การดูดซับของโมเลกุลชนิดเดียวบนพื้นผิว
โดยไม่มีการแตกตัวของโมเลกุลที่ถูกดูดซับ
พิจารณาแก๊ส
A
ที่ความดัน
PA
ที่ดูดซับลงบนพื้นผิวโดยไม่เกิดการแตกตัว
กำหนดให้สัดส่วนของพื้นผิวที่ถูกปกคลุมไว้ด้วยแก๊ส
A
คือ
θA
(พื้นที่ที่
A
ปกคลุมต่อพื้นที่ผิวทั้งหมดหรือ
surface
coverage) ดังนั้นที่สภาวะสมดุล
ที่สภาวะคงตัว
อัตราทั้งสองจะเท่ากัน
ดังนั้นเราจะได้
เมื่อ
KA
คือค่าคงที่สมดุลของการดูดซับ
ซึ่งเท่ากับ k/k'
รูปที่
๑
ตัวอย่างกราฟความสัมพันธ์ระหว่างความดันกับสัดส่วนพื้นที่ผิวที่ถูกปกคลุมที่ค่า
KA
ต่าง
ๆ กันในกรณีที่โมเลกุลที่ลงมาดูดซับนั้นไม่เกิดการแตกตัว
(ข)
การดูดซับของโมเลกุลสองชนิดบนพื้นผิวเดียวกัน
โดยที่ไม่มีการแตกตัวของโมเลกุลที่ถูกดูดซับ
ในกรณีนี้จะพิจารณาแก๊ส
A
และ
B
ที่แย่งกันดูดซับบนพื้นผิวเดียวกัน
(competitive
adsorption) โดยที่ทั้งโมเลกุลแก๊ส
A
และแก๊ส
B
ไม่มีการแตกตัว
กำหนดให้สัดส่วนของพื้นผิวที่ถูกปกคลุมไว้ด้วยแก๊ส
A
คือ
θA
(พื้นที่ที่
A
ปกคลุมต่อพื้นที่ผิวทั้งหมด)
สัดส่วนของพื้นผิวที่ถูกปกคลุมไว้ด้วยแก๊ส
B
คือ
θB
(พื้นที่ที่
B
ปกคลุมต่อพื้นที่ผิวทั้งหมด)
ดังนั้นที่สภาวะสมดุล
ที่สภาวะสมดุล
อัตราการดูดซับ A
จะเท่ากับอัตราการคายซับ
A
และอัตราการดูดซับ
B
จะเท่ากับอัตราการคายซับ
B
ดังนั้นเราจะได้
จัดรูปแบบสมการใหม่โดยให้
KA
= kA/k'A
และ
KB
= kB/k'B
จะได้
โดยการแทนค่า
θB
จากสมการ
(12)
ลงในสมการ
(11)
และแทนค่า
θA
จากสมการ
(11)
ลงในสมการ
(12)
จะได้
(ค)
การดูดซับของโมเลกุลชนิดเดียวบนพื้นผิว
โดยโมเลกุลที่ถูกดูดซับมีการแตกตัว
พิจารณากรณีโมเลกุล
A2
ซึ่งเมื่อเกิดการดูดซับบนพื้นผิวจะแตกออกกลายเป็น
A
สองอะตอม
เกาะบนพื้นผิวสองตำแหน่งตามสมการ
A2
+ 2θ
→
2θA
ที่สภาวะคงตัว
อัตราทั้งสองจะเท่ากัน
ดังนั้นเราจะได้
Langmuir
isotherm มีข้อจำกัดหลายประการ
ทั้งนี้เนื่องจากข้อเท็จจริงมีสิ่งที่ขัดกับข้อสมมุติที่ได้ตั้งไว้ดังนี้
1.
มีแรงกระทำระหว่างกันระหว่างโมเลกุลที่ลงมาเกาะบนพื้นผิว
ระหว่างโมเลกุลที่อยู่เคึยงข้างกัน
หรือระหว่างโมเลกุลที่ถูกดูดซับอยู่ก่อนกับโมเลกุลที่กำลังจะถูกดูดซับ
2.
พื้นผิวที่เตรียมขึ้นมักจะมีความไม่สม่ำเสมออยู่ในตัว
ทำให้ตำแหน่งดูดซับนั้นไม่เหมือนกันทุกตำแหน่ง
3.
รูปแบบการดูดซับระหว่างโมเลกุลที่ลงมาเกาะกับพื้นผิวของของแข็ง
อาจมีได้หลายรูปแบบ
โดยบางโมเลกุลนั้นอาจถูกดูดซับในรูปแบบ
1
โมเลกุลต่อ
1
ตำแหน่ง
หรือ 1
โมเลกุลต่อหลายตำแหน่งก็ได้
ข้อเท็จจริงสองข้อแรกทำให้เกิดการเปลี่ยนแปลงพลังงานของการดูดซับ
โดยโมเลกุลแรกๆที่ลงมาดูดซับจะมีการเปลี่ยนแปลงพลังงานมากที่สุด
และการเปลี่ยนแปลงพลังงานนี้จะลดลงเมื่อจำนวนโมเลกุลที่อยู่บนพื้นผิวมากขึ้น
แต่ถึงกระนั้นก็ตามจากการทดลองพบว่าการดูดซับที่ปกคลุมพื้นผิวไม่เกิน
1
ใน
3
สามารถอธิบายได้ด้วยแบบจำลองนี้ได้ดี
รูปที่
๒
ตัวอย่างกราฟความสัมพันธ์ระหว่างความดันกับสัดส่วนพื้นที่ผิวที่ถูกปกคลุมที่ค่า
KA
ต่าง
ๆ กันในกรณีที่โมเลกุลที่ถูกดูดซับเกิดการแตกตัว
(ง)
การคำนวณหาพื้นที่ผิวโดยใช้แบบจำลองไอโซเทอมการดูดซับของ
Langmuir
สัดส่วนของพื้นผิวที่ถูกปกคลุมไว้ด้วยแก๊ส
A
หรือ
θA
นั้นมีค่าเท่ากับ
Vads/Vm
เมื่อ
Vads
คือปริมาตรแก๊สที่ถูกดูดซับต่อหน่วยน้ำหนักของสารดูดซับ
และ Vm
คือปริมาตรแก๊สที่ถูกดูดซับเมื่อแก๊สนั้นปกคลุมพื้นผิวเอาไว้ทั้งหมดด้วยชั้นโมเลกุลเพียงชั้นเดียว
(monolayer)
ดังนั้นเมื่อแทนค่า
Vads/Vm
ลงในสมการที่
(4)
จะได้
กล่าวคือถ้าเราเขียนกราฟโดยใช้
PA
เป็นแกน
x
และค่า
(PA/Vads)
เป็นแกน
y
จะได้กราฟที่มีความดันเท่ากับ
1/Vm
และตัดแกน
y
ที่ตำแหน่ง
y
= 1/(KAVm)
จากค่าความชันของกราฟ
(1/Vm)
จะทำให้เราสามารถคำนวณค่าปริมาตรแก๊สที่ถูกดูดซับเมื่อแก๊สนั้นปกคลุมพื้นผิวเอาไว้ทั้งหมดด้วยชั้นโมเลกุลเพียงชั้นเดียว
ซึ่งนำไปสู่การคำนวณหาค่าจำนวนโมเลกุลของแก๊สที่ต้องใช้ในการปกคลุมพื้นผิวเอาไว้ทั้งหมดด้วยชั้นโมเลกุลเพียงชั้นเดียว
และถ้าเราทราบพื้นที่หน้าตัดของโมเลกุลนั้น
(เช่นโมเลกุลของ
N2
ที่อุณหภูมิ
-196ºC
(อุณหภูมิจุดเดือดของไนโตรเจนเหลวที่ความดันบรรยากาศ)
มีพื้นที่หน้าตัด
0.154
ตารางนาโนเมตรต่อโมเลกุล)(๑)
เราก็จะคำนวณหาค่าพื้นที่ผิวของสารดูดซับได้จากผลคูณระหว่างพื้นที่หน้าตัดของ
1
โมเลกุลกับจำนวนโมเลกุลของแก๊สที่ต้องใช้ในการปกคลุมพื้นผิวเอาไว้ทั้งหมดด้วยชั้นโมเลกุลเพียงชั้นเดียว
หมายเหตุ
(๑)
Livingston, H.K., "The cross-sectional areas of molecules
adsorbed on solid surfaces", Journal of Colloid Science Volume
4, Issue 5, October 1949, Pages 447–458.
รูปที่ ๓
Irvin
Langmuir ผู้ได้รับรางวัลโนเบลสาขาเคมีในปีค.ศ.
๑๙๓๒
(พ.ศ.
๒๔๗๕)
เกิด
31
มกราคมปีค.ศ.
๑๘๘๑
ถึงแก่กรรม ๑๖ สิงหาคมปีค.ศ.
๑๙๕๗
รูปจาก
http://www.nobelprize.org/nobel_prizes/chemistry/laureates/1932/langmuir.html