"Probe
molecule ที่ดีที่สุดก็คือตัวโมเลกุลสารตั้งต้นเอง"
น่าจะเป็นข้อสรุปที่ดีสำหรับเกณฑ์ข้อที่สี่ของ
Lercher
และคณะที่กล่าวไว้
"ขนาดของ
Probe
molecule
ที่จะใช้วัดความหนาแน่นของตำแหน่งที่เป็นกรดควรที่จะมีขนาดประมาณเทียบเคียงกับขนาดของสารตั้งต้นของปฏิกิริยาที่ศึกษา"
("ความหนาแน่น"
นี้คือบนพื้นผิวของแข็งนะ)
ปฏิกิริยาที่เกิดบนตัวเร่งปฏิกิริยาวิวิธพันธ์นั้นจะเกิดขึ้นในรูพรุนของตัวเร่งปฏิกิริยา
ซึ่งรูพรุนนี้มีทั้งขนาดเล็กและขนาดใหญ่
ปฏิกิริยาจะเกิดขึ้นได้ก็ต่อเมื่อสารตั้งต้นสามารถลงไปเกาะยังตำแหน่งที่ว่องไว
(เช่นตำแหน่งที่เป็นกรดในกรณีของปฏิกิริยาที่ต้องการกรดในการเร่งปฏิกิริยา)
ตำแหน่งที่เป็นกรดนี้มีอยู่ทั้งบนพื้นผิวของรูพรุนขนาดเล็กและรูพรุนขนาดใหญ่
แต่ตำแหน่งที่เป็นกรดที่สามารถเร่งปฏิกิริยาได้จะต้องเป็นตำแหน่งที่โมเลกุลสารตั้งต้นเข้าถึงได้
ถ้าสารตั้งต้นมีขนาดโมเลกุลเล็ก
มันก็สามารถแพร่เข้าไปถึงตำแหน่งที่เป็นกรดที่อยู่ในรูพรุนชนาดเล็กได้
แต่ถ้าสารตั้งต้นมีขนาดโมเลกุลใหญ่
มันจะไม่สามารถใช้ประโยชน์จากตำแหน่งที่เป็นกรดที่อยู่ในรูพรุนขนาดเล็กได้
คาร์บอนมอนอกไซด์หรือ
CO
(kinetic parameter = 0.073 nm) และแอมโมเนียหรือ
NH3
(kinetic parameter = 0.073 nm)
เป็นโมเลกุลที่มีขนาดเล็กที่สามารถเข้าไปถึงตำแหน่งที่เป็นกรดที่อยู่ในรูพรุนขนาดเล็กได้
โดยเฉพาะ NH3
มักจะถูกใช้เพื่อการวัดปริมาณตำแหน่งที่เป็นกรดทั้งหมดบนพื้นผิว
แต่ถ้าสารตั้งต้นของปฏิกิริยาที่สนใจนั้นมีขนาดโมเลกุลใหญ่จนไม่สามารถแพร่เข้าไปในรูพรุนขนาดเล็กได้
จะมีเฉพาะตำแหน่งที่เป็นกรดที่อยู่ในรูพรุนขนาดใหญ่เท่านั้นที่มีบทบาทในการทำให้เกิดปฏิกิริยา
(พวกที่อยู่ในรูพรุนขนาดเล็กไม่มีประโยชน์ใด
ๆ เพราะสารตั้งต้นแพร่เข้าไปไม่ถึง)
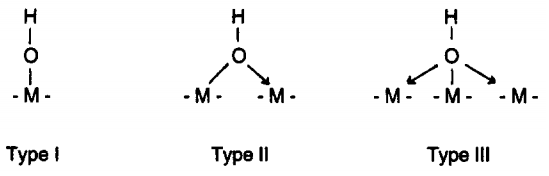
ดังนั้นในกรณี
รูปที่
๑ สารพวก substituted
pyridine หรือไพริดีนที่มีหมู่แทนที่ตรงตำแหน่งอะตอม
C
ที่อยู่ด้านข้างอะตอม
N
เช่น
2,6-Dimethylpyridine
และ
2,6-Di-t-butylpyridine
ไม่เพียงแต่จะมีประโยชน์ในการวัดปริมาณตำแหน่งกรด
Brönsted
แต่ยังมีประโยชน์ในการวัดตำแหน่งที่เป็นกรดในรูพรุนขนาดใหญ่ที่สารตั้งต้นที่มีขนาดโมเลกุลใหญ่สามารถเข้าถึงได้
ก่อนที่เราจะไปคุยกันเรื่องนี้อยากให้ลองพิจารณาสเปกตรัมการดูดกลืนรังสีอินฟราเรดของ
2,6-dimethylpyridine
บนพื้นผิว
γ-Al2O3
ที่ผ่านการให้ความร้อนที่อุณหภูมิ
400ºC
(รูปที่
๒)
และ
500ºC
(รูปที่
๓)
ในสุญญากาส
ก่อนทำการดูดซับดูก่อนนะครับ
สิ่งที่อยากให้ดูก็คือผลของอุณหภูมิที่ใช้ในการเตรียมตัวอย่างก่อนทำการวัด
แนวเส้นประสีแดงในรูปที่
๓ นั้นคือแนวเส้น base
line ที่มันไต่ขึ้นสูงเรื่อย
ๆ ในช่วงเลขคลื่นสูง
ลักษณะเช่นนี้เกิดจากการที่อนุภาคตัวอย่างนั้นมีขนาดใหญ่เกินกว่าความยาวคลื่นแสง
ทำให้รังสีที่ตกกระทบนั้นมีการสะท้อนออกไปส่วนหนึ่ง
จึงทำให้เห็นค่า absorbance
ช่วงเลขคลื่นสูงมีค่าสูงขึ้น
แต่นั่นเป็นเพราะรังสีช่วงนี้ถูกสะท้อนออกไป
ไม่ได้หายไปเพราะถูกดูดกลืน
รูปที่ ๒ สเปกตรัมการดูดกลืนรังสีอินฟราเรดของ 2,6-dimethylpyridine บนพื้นผิว γ-Al2O3 ที่ผ่านการให้ความร้อนที่อุณหภูมิ 400ºC ในสุญญากาศก่อนทำการดูดซับ เส้นประ a คือเส้นก่อนจะมีการดูดซับ 2,6-dimethylpyridine
รูปที่ ๒ สเปกตรัมการดูดกลืนรังสีอินฟราเรดของ 2,6-dimethylpyridine บนพื้นผิว γ-Al2O3 ที่ผ่านการให้ความร้อนที่อุณหภูมิ 400ºC ในสุญญากาศก่อนทำการดูดซับ เส้นประ a คือเส้นก่อนจะมีการดูดซับ 2,6-dimethylpyridine
รูปที่
๓ สเปกตรัมการดูดกลืนรังสีอินฟราเรดของ
2,6-dimethylpyridine
บนพื้นผิว
γ-Al2O3
ที่ผ่านการให้ความร้อนที่อุณหภูมิ
500ºC
ในสุญญากาศก่อนทำการดูดซับ
เส้นประ a
คือเส้นก่อนจะมีการดูดซับ
2,6-dimethylpyridine
เช่นกัน
พึงสังเกตความแตกต่างระหว่างเส้น
a
ในรูปที่
๒ และ ๓
เคยมีคนมาถามผมเกี่ยวกับการวัดการดูดกลืนรังสีอินฟราเรดของไพริดีนเพื่อวัดปริมาณตำแหน่งกรด
Brönsted
และ
Lewis
บนพื้นผิวของแข็ง
เพื่อที่จะดูว่าตำแหน่งกรดแบบไหนสำคัญต่อการเกิดปฏิกิริยา
(เขาคงมาถามในฐานะที่เขาคงรู้ว่าผมเคยลงมือทำการทดลองนี้ด้วยตัวเอง
ตั้งแต่การเตรียมแผ่น wafer
การป้อนไพริดีนให้ตัวอย่างดูดซับ
ไปจนถึงการเก็บสเปกตรัมการดูดกลืน)
ซึ่งผมก็ตอบเขาไปว่า
"อยากให้ผลออกมาแบบไหนล่ะ
จัดให้ได้"
เพราะจากประสบการณ์ที่เคยลองถูกลองผิดในช่วงแรกมันทำให้รู้ว่า
ธรรมชาติของตัวอย่าง
(คือจับความชื้นได้ดีแค่ไหน)
ประสบการณ์ของตัวอย่าง
(กล่าวคือสัมผัสอากาศที่มีความชื้นสูงแค่ไหนมานานขนาดไหนก่อนนำมาวัด)
และการเตรียมตัวอย่างก่อนให้ดูดซับ
probe
molecule
(ระยะเวลาและอุณหภูมิที่ใช้ในขั้นขั้นตอนการทำสุญญากาศและให้ความร้อนเพื่อกำจัดแก๊สต่าง
ๆ ที่อยู่ในรูพรุนและที่พื้นผิวดูดซับเอาไว้)
มันส่งผลต่อตำแหน่งกรด
Brönsted
ที่จะวัดได้
การทำใช้อุณหภูมิสูงทำให้หมู่
-OH
หายไปจากพื้นผิวมากกว่าการใช้อุณหภูมิที่ต่ำกว่า
และนั่นอาจหมายถึงการมีตำแหน่งกรด
Lewis
ปรากฏเพิ่มมากขึ้น
(-OH
สองหมู่หลอมรวมกันกลายเป็นโมเลกุลน้ำหลุดออกไป
ไอออนบวกที่เดิมมีหมู่ -OH
เกาะอยู่ก็เลยเปิดออก)
ผลการวัดในรูปที่
๒ และ ๓ นั้นนำมาจากบทความในรูปที่
๔ ข้างล่างที่ให้คำอธิบายไว้ว่าการเพิ่มอุณหภูมิการเตรียมตัวอย่างจาก
400ºC
เป็น
500ºC
(ทำในสุญญากาศ)
ทำให้หมู่
-OH
บนพื้นผิวมีการจัดโครงสร้างใหม่
โดย γ-Al2O3
ที่ผ่านการความร้อนที่
500ºC
มีปริมาณตำแหน่งกรด
Brönsted
ที่มีความแรงสูงมากกว่า
และมีตำแหน่งกรด Brönsted
ที่มีความแรงต่ำน้อยกว่าเมื่อเทียบกับ
γ-Al2O3
ที่ผ่านการความร้อนที่
400ºC
จากประสบการณ์ที่เคยมี
ปรากฏการณ์นี้จะเด่นชัดสำหรับพื้นผิวของแข็งที่มีปริมาณ
-OH
สูง
รูปที่
๔ บทความที่เป็นต้นเรื่องของรูปที่
๒ และ ๓
เทคนิคดั้งเดิมที่ใช้ปฏิกิริยาทดสอบเพื่อหาว่ากรดบนพื้นผิวตัวเร่งปฏิกิริยานั้นมีความแรงสูงถึงระดับไหน
แม้ว่าจะเป็นวิธีการที่วุ่นวายและไม่ให้สเกลความแตกต่างที่เด่นชัด
เช่นตัวเร่งปฏิกิริยา A
และ
B
สามารถทำให้เกิดปฏิกิริยา
alcohol
dehydration ได้
แต่ B
สามารถทำให้เกิดปฏิกิริยา
alkylation
of aromatics ก็แสดงว่า
B
เป็นกรดที่แรงกว่า
A
ในทำนองเดียวกันถ้า
C
สามารถทำให้เกิดปฏิกิริยา
paraffin
cracking ได้แต่
B
ทำไม่ได้
ก็แสดงว่า C
เป็นกรดที่แรงกว่า
B
แต่มันก็ไม่ได้บอกว่าความแตกต่างระหว่าง
A
กับ
B
และ
B
กับ
C
นั้นแตกต่างกันมากแค่ไหน
แต่วิธีนี้ก็มีข้อดีคือด้วยการเลือกโมเลกุลสารตั้งต้นที่มีขนาดใกล้เคียงกับสารตั้งต้นในปฏิกิริยาที่เราสนใจ
มันจะบ่งบอกถึงตำแหน่งกรดที่สารตั้งต้นในปฏิกิริยาที่เราสนใจนั้นสามารถแพร่เข้าถึงได้
(หมายเหตุ
:
ตัวอย่างปฏิกิริยาทดสอบที่ต้องการกรดที่มีความแรงจากต่ำไปสูงได้แก่
Dehydration
of alcohols < Cis-trans isomerisation of olefins < Double-bond
migration < Alkylation of aromatics < Isomerisation of
alkylaromatics < Transalkylation of alkylaromatics < Cracking
of alkylaromatics < Skeletal isomerisation < Cracking of
paraffins จาก
Satterfield,C.N.,"Heterogeneous
catalysis in industrial practice", 2nd Ed.,McGraw Hill, 1991)
รูปที่
๕ บทความที่วัดความเป็นกรดบนพื้นผิวด้วยการใช้
probe
molecule ที่มีขนาดแตกต่างกัน
โดยพบว่าในกรณีของปฏิกิริยา
catalytic
cracking สารตั้งต้นที่มีขนาดใหญ่เช่น
1,3,5-Triisopropylbenzene
ปริมาณกรดที่วัดด้วย
probe
molecule ที่มีขนาดใหญ่คือ
2,6-Di-t-butylpyridine
จะสอดคล้องกับความว่องไวในการเกิดปฏิกิริยาที่วัดได้
บทความในรูปที่
๕ เป็นตัวอย่างหนึ่งของการใช้
probe
molecule ที่มีขนาดต่าง
ๆ กันในการวัดปริมาณตำแหน่งกรดบนพื้นผิว
โดยพบว่า probe
molecule
ที่มีขนาดใหญ่จะวัดได้เฉพาะตำแหน่งกรดที่อยู่บริเวณผิวนอกและเป็นตำแหน่งที่โมเลกุลสารตั้งต้นขนาดใหญ่สามารถใช้ประโยชน์ในการทำปฏิกิริยาได้
กล่าวโดยสรุปก็คือ
การมีตำแหน่งที่เป็นกรดที่มีความแรงที่เหมาะสมสำหรับปฏิกิริยาที่ต้องการในปริมาณมากนั้น
ไม่ได้ทำให้ตัวเร่งปฏิกิริยานั้นเป็นตัวเร่งปฏิกิริยาที่ดีเสมอไป
เพราะมันต้องอยู่ในตำแหน่งที่โมเลกุลสารตั้งต้นนั้นสามารถเข้าถึงได้ด้วย
ดังนั้นการแปลผลความสัมพันธ์ระหว่าง
ปริมาณ-ความแรงของตำแหน่งที่เป็นกรด
(ที่วัดได้ด้วยการใช้
probe
molecule ขนาดเล็ก)
กับอัตราการเกิดปฏิกิริยา
จึงอาจไม่ให้ภาพที่ถูกต้องเสมอไปถ้าหากโมเลกุลสารตั้งต้นมีขนาดใหญ่
การนำเอาผลการกระจายขนาดรูพรุนและรูพรุนเฉลี่ยมาพิจารณาประกอบจึงอาจให้ภาพที่ถูกต้องมากกว่า